Comprendre l’importance de la thérapie par compression dans la prévention de la TEV
Lorsque nous avons une petite blessure, nous faisons souvent l’éloge de la capacité de notre sang à coaguler pour protéger la plaie et éviter une perte de sang supplémentaire. Cependant, lorsque le sang commence à coaguler au mauvais endroit et au mauvais moment, les conséquences peuvent changer la vie, voire être fatales. Chaque année, les caillots de sang dans les veines profondes causent de grandes souffrances à des millions de personnes. Dans cet article, nous examinons en détail les caillots sanguins, leurs causes et la façon dont le système de compression active Flowtron peut aider à prévenir cette affection.
« On estime à dix millions le nombre de cas de thrombo-embolie veineuse (TEV) observés chaque année dans le monde. Il s’agit d’une maladie potentiellement mortelle qui peut entraîner une charge financière importante pour le personnel soignant en soins intensifs et les systèmes de soins médicaux », explique Henrik Runnerström, Directeur mondial de la Gestion des catégories de produits, Prévention de la TEV chez Arjo.
Près de 30 pour-cents des patients décèdent dans les 30 jours suivant l’apparition de la TEV, tandis que 25 pour-cents des décès inattendus de patients hospitalisés sont liés à une embolie pulmonaire lors de l’autopsie1.
Environ un tiers des patients souffrant de thrombose veineuse profonde (TVP) développent un syndrome post-thrombotique qui provoque souffrance, tuméfaction et douleur1. Pour 25 % de ces patients2, l’ulcération chronique qui en résulte est associée à un coût substantiel du traitement en cours3.
Henrik poursuit : « Outre la souffrance humaine, le nombre élevé de cas de TEV se traduit par une charge financière importante pour le personnel soignant en soins intensifs et les systèmes de soins médicaux. »
Qu’est-ce que la TEV ?
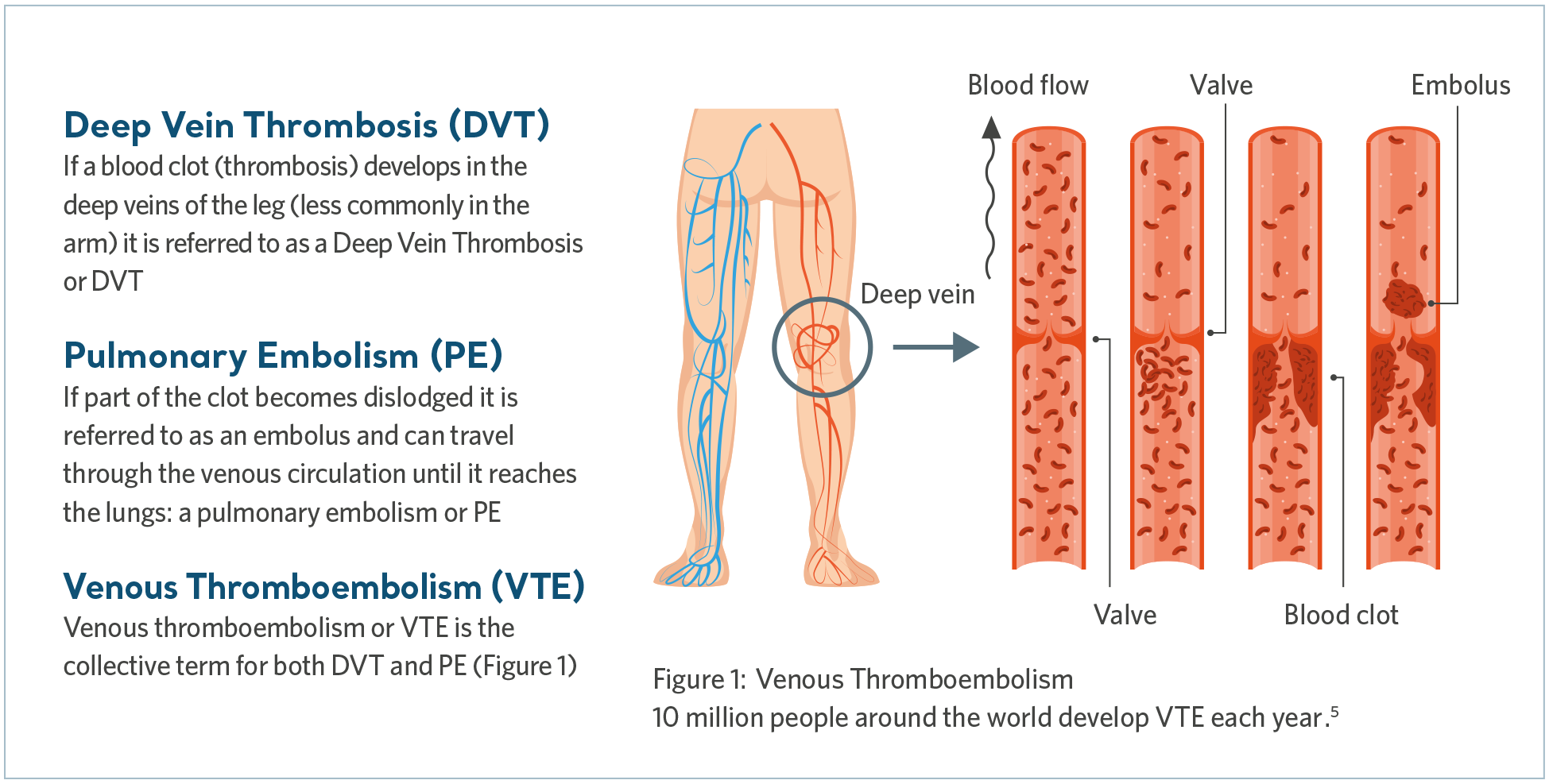
La thrombo-embolie veineuse (TEV) est le terme générique qui désigne la thrombose veineuse profonde (TVP) ainsi que l’embolie pulmonaire (EP). Une TVP se produit lorsqu’un caillot sanguin se forme dans une veine profonde, le plus souvent dans la jambe, tandis qu’une EP peut survenir si le caillot se détache et se déplace vers les poumons, bloquant une partie ou la totalité de l’apport sanguin.
L’embolie pulmonaire est une affection potentiellement mortelle4. Bien que le diagnostic et le traitement précoces de la TEV puissent mener à une guérison, des complications à long terme peuvent entraîner un traitement et des souffrances à vie.
Quelles sont les causes de la TEV ?
La TEV se déclenche lorsque plusieurs facteurs de risque, désignés collectivement sous le nom de « triade de Virchow », influencent l’homéostasie et entraînent la formation de caillots.6 Examinons chacun des éléments qui composent la triade de Virchow.
Triade de Virchow
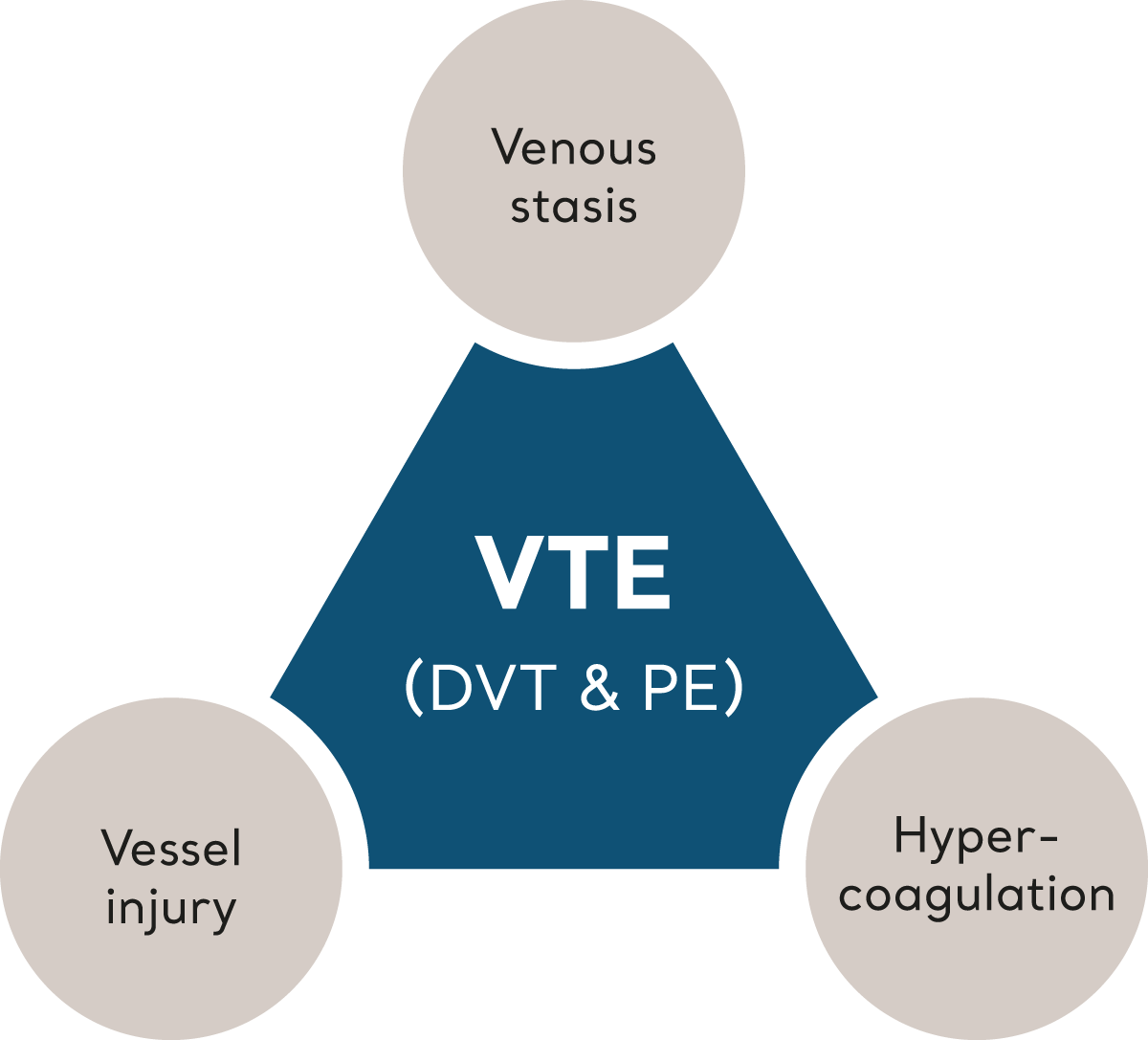
Stase veineuse
Les conditions qui ralentissent la circulation sanguine (stase) dans les veines profondes augmenteront le risque de TEV. L’immobilité, peut-être due à l’âge, à la fragilité ou à l’alitement, constitue un véritable facteur de risque.
L’obstruction physique des vaisseaux sanguins, découlant de forces externes ou de la pression exercée par des tumeurs et les ganglions lymphatiques, pèse également dans la balance, à l’instar de TVP antérieures.
Hypercoagulation
Les changements de densité et de chimie sanguines peuvent favoriser la formation de caillots. Ces derniers sont associés à des conditions allant de la simple déshydratation à l’hypoxie, aux tumeurs malignes et aux traumatismes, en passant par les traitements hormonaux, les maladies inflammatoires et les prédispositions génétiques.
Lésion des vaisseaux
Des lésions peuvent survenir lors d’un accident ou d’interventions médicales telles que des procédures chirurgicales ou invasives. Lorsqu’une lésion apparaît, une série physiologique normale d’événements amorce l’adhésion des plaquettes et l’éventuelle formation d’un caillot sanguin ; ce mécanisme de protection referme la lésion et lance le processus de cicatrisation. Cependant, dans certains cas, ce processus est excessif ou inapproprié.
Quelles sont les personnes exposées au risque de TEV ?
Les patients hospitalisés pour une intervention chirurgicale constituent un groupe à risque particulier7, puisque cette dernière augmente le risque en raison des anesthésiants (hypercoagulabilité) et des myorelaxants (stase) administrés ou encore des éventuelles lésions causées aux vaisseaux du fait de l’intervention chirurgicale
. Il est également évident que les patients qui n’ont pas subi d’interventions chirurgicales présentent un risque élevé de TEV.
Henrik Runnerström déclare : « Il existe de nombreux facteurs contribuant à la TEV et, même si cette affection est souvent associée aux personnes immobiles et aux personnes âgées, elle peut également survenir à des personnes apparemment en bonne santé, en bonne forme physique et athlétiques. »
L’ancien joueur de hockey d’élite Stefan Elvenes en Suède en est un exemple. Quelques mois après avoir pris sa retraite, après 22 ans de carrière au plus haut niveau en Suède et au Danemark, il a remarqué un gonflement à l’arrière de sa jambe gauche.
« Lorsque le médecin m’a dit qu’il s’agissait d’un caillot de sang, je n’arrivais pas à y croire. Je n’avais que 37 ans et j’étais encore en pleine forme. Je n’étais pas censé souffrir d’une telle chose », explique Stefan.
Après avoir été informé que les jeunes et les sportifs pouvaient également développer des caillots sanguins, Stefan a été traité avec succès à l’aide d’anticoagulants. Cependant, trois semaines après avoir cessé de prendre ses médicaments, il a subi une crise d’angoisse sévère.
« Au fond de moi, l’arrêt de mon traitement se traduisait par un risque de formation d’un nouveau caillot sanguin. Cela a probablement déclenché mes crises d’angoisse », explique Stefan. « Je suis resté longtemps comme une loque mentalement. Mais une thérapie régulière chez un psychologue m’a permis de surmonter mes angoisses. Aujourd’hui, j’ai retrouvé la paix. »
Découvrez l’histoire de Stefan ici
Prévention de la TEV
La prophylaxie pharmacologique, comme les anticoagulants administrés à Stefan, est l’un des moyens de traiter la TEV. Les stratégies préventives font également appel à diverses méthodes mécaniques, telles que la compression pneumatique intermittente (CPI) et les bas de contention gradués passifs (BCG).
La CPI est une intervention très bien établie et éprouvée, présentant des données factuelles convaincantes et peu d’effets secondaires. Elle est indiquée chez un large éventail de patients hospitalisés à risque de TEV.
L’objectif de la CPI est de faire circuler le sang depuis les veines les plus profondes par le gonflage et le dégonflage intermittents d’une attelle reliée à une pompe électrique.
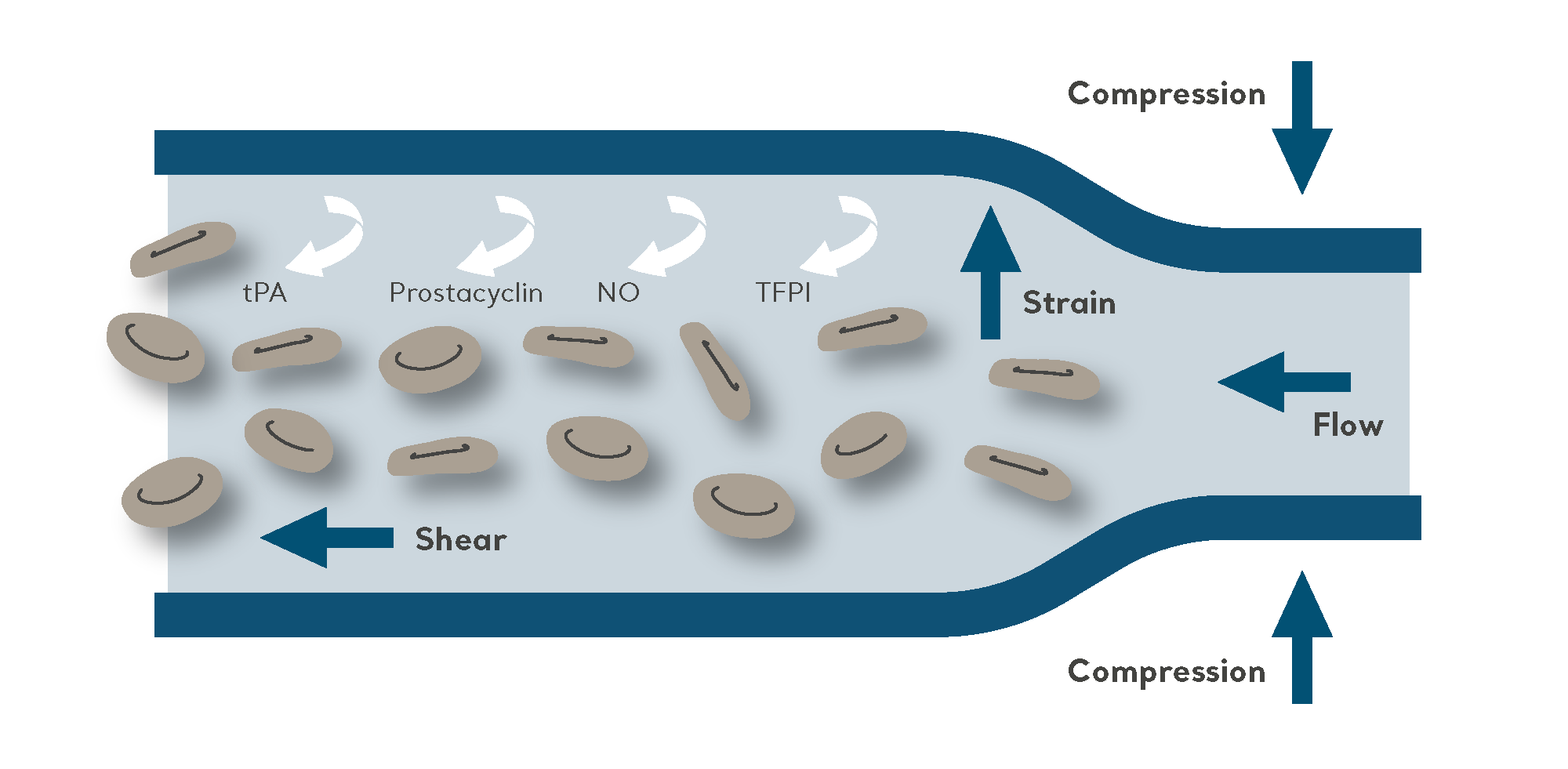
À l’instar d’une méthode mécanique non invasive de prophylaxie de la TEV, la CPI s’avère efficace lorsqu’elle est employée comme technique de prévention unique, comme pour les patients présentant un risque élevé d’hémorragie. Elle est également souvent employée avec une prophylaxie pharmacologique chez les patients à haut risque (pour réduire davantage le risque de TEV).
Un partenaire de confiance pour l’utilisation de la CPI dans le domaine de la prévention de la TEV
Depuis les années 1970, les études sur la TEV ont clairement démontré les effets préventifs de la CPI des veines profondes de la jambe. Depuis lors, Arjo a joué un rôle déterminant dans la mise au point de systèmes de CPI simples d’utilisation et efficaces d’un point de vue clinique et ce, afin d’aider les établissements de soins de santé aux quatre coins du monde. La gamme de systèmes de compression active Flowtron est conçue pour améliorer l’efficacité clinique grâce à son confort, sa facilité d’utilisation et sa rentabilité.
Arjo s’engage également à améliorer la qualité des soins prodigués aux patients et à aider les professionnels de santé à lutter contre la thrombose veineuse profonde et l’embolie pulmonaire.
« Notre engagement va au-delà de la fourniture de pompes et d’attelles incluses dans notre système de compression active Flowtron. Nous voulons distinguer Arjo de la concurrence en étant un partenaire qui ajoute des services et des connaissances précieuses à notre offre », déclare Henrik Runnerström.
Il poursuit : « Même si les professionnels de santé sont conscients des risques, ils peuvent manquer de temps, de formation et de ressources nécessaires pour optimiser leurs stratégies de prévention. La compréhension de ces difficultés est la base de l’élaboration de nos services et programmes de formation, qui sont conçus pour renforcer la capacité à prévenir et traiter la TEV. »
Le système de compression active Flowtron – une véritable solution prête à l’emploi
La solution d’Arjo, le système de compression active Flowtron, utilise une pompe pneumatique pour gonfler les attelles autour du pied, du mollet, de la cuisse ou une combinaison des trois.
Henrik explique : « En imitant l’action de la pompe musculaire du mollet, la CPI augmente la circulation sanguine dans les veines profondes et contribue à prévenir la coagulation du sang. Il s’agit d’un traitement bien établi et éprouvé avec une base probante convaincante. »

La pompe Flowtron ACS900 (photo ci-dessus) permet une compression homogène et séquentielle via différents types d’attelles. Grâce à la reconnaissance automatique de l’attelle SmartSenseTM (voir la photo ci-dessous) et au démarrage à l’aide d’un seul bouton, Flowtron est une véritable solution prête à l’emploi.
« La flexibilité réduit le besoin de plusieurs modèles de pompe dans l’établissement de soins », explique Henrik. « Le système est facile à configurer et à utiliser et la batterie intégrée permet une thérapie ininterrompue, même lorsque la pompe n’est pas branchée à une prise électrique. »
Il poursuit : « Avec notre gamme d’attelles, le système est confortable pour le patient, commode pour le professionnel de la santé et cliniquement efficace pour fournir une compression pneumatique intermittente, ce qui contribue à améliorer l’observance des soins pour tous les patients. »
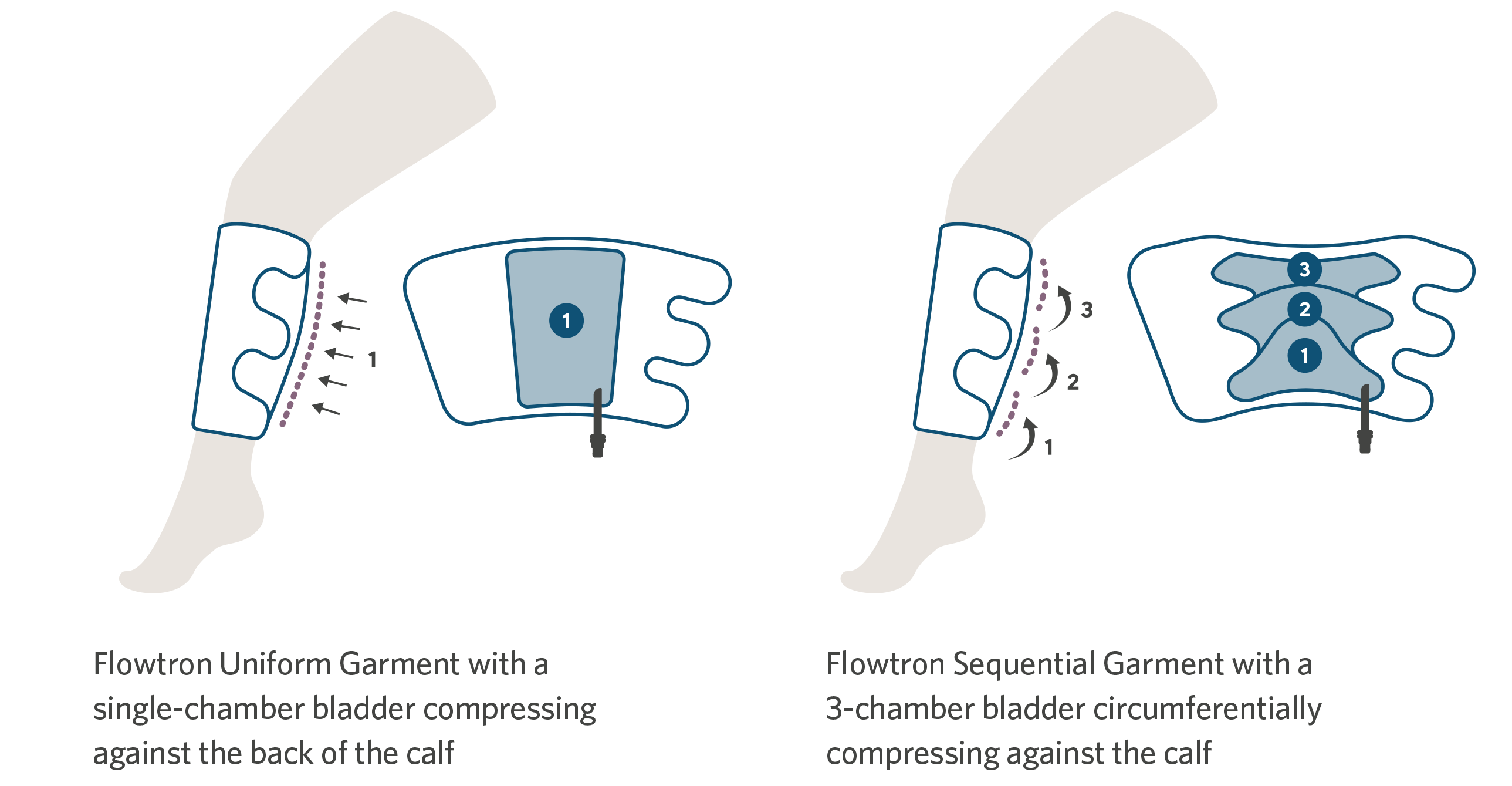
Pour garantir un confort optimal, la gamme Flowtron propose un large choix d’attelles, de toutes les tailles, en versions adaptées au mollet ou à la cuisse, assurant une compression séquentielle ou uniforme. La compression du pied est disponible en taille normale ou grande. Une combinaison de différentes attelles peut être utilisée simultanément. Le choix de l’attelle dépend simplement du choix du praticien.
Henrik Runnerström explique : « Les directives internationales recommandent un traitement continu pendant 18 à 24 heures par jour8. Des études montrent un lien direct entre le niveau de confort et la volonté des patients de porter des attelles plus longtemps9. Notre objectif est d’améliorer le confort du patient en utilisant des tissus respirants, qui aident à maintenir le patient au sec et au frais en laissant passer la chaleur et l’humidité. »
Pour en savoir plus sur le système de compression active Flowtron, cliquez ici
Flowtron CPI – données cliniques
Études de laboratoire
Nombre d’études de recherche appuyant la compression pneumatique intermittente comme forme générique de la prophylaxie de la TEV portaient sur des versions antérieures des dispositifs de la gamme Flowtron actuelle. Même si la technologie a été améliorée, les principes de conception sous-jacents, tels que la pression de cycle, le taux de gonflage et les intervalles de cycle, demeurent identiques.
Parmi les études démontrant l’effet antithrombotique et profibrinolytique de la CPI, les principales conclusions suggèrent que la CPI réduit la probabilité de formation de caillots. En outre, la CPI limite également la formation de caillots et décompose les caillots lorsqu’ils commencent à se former.7
Les principales conclusions de ces études sont que la CPI réduit la probabilité de formation de caillots, limite également la formation de caillots et les décompose lorsqu’ils commencent à se former.
Études comparatives sur la circulation sanguine
L’inversion de la stase veineuse jouant un rôle clé dans la prévention, la gamme de dispositifs de CPI Flowtron a été soumise à de nombreux tests comparatifs effectués en laboratoire et a continuellement démontré des résultats favorables10,11. Voir le tableau ci-dessous.
Données de laboratoire
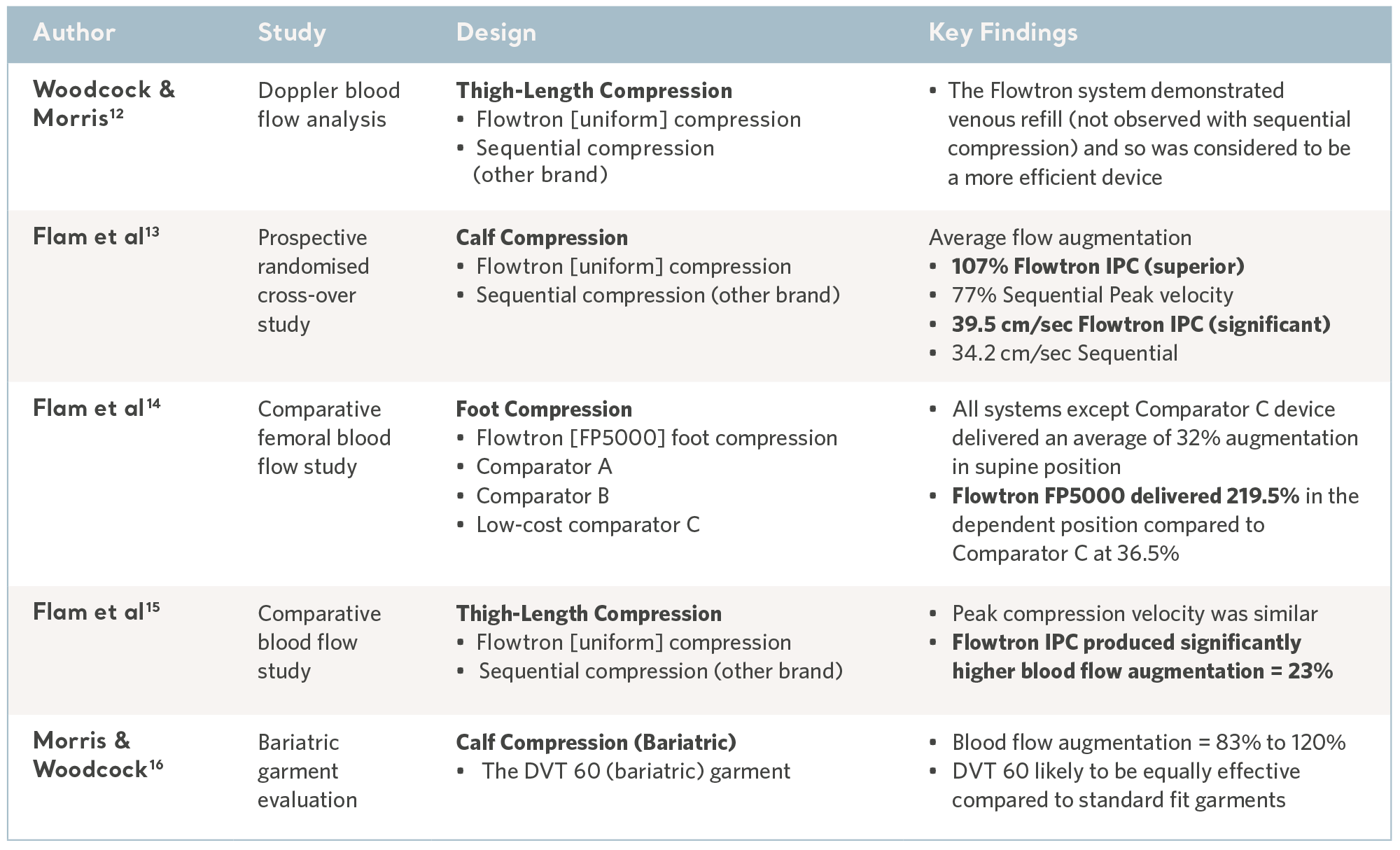
Efficacité clinique
Au cours des 30 dernières années, des experts indépendants ont mené de nombreuses études cliniques. Les sujets ont été recrutés dans des populations de patients présentant les plus hauts risques et parmi un éventail de spécialités cliniques. Les résultats ont systématiquement démontré la capacité prophylactique de la gamme de dispositifs de CPI Flowtron lorsqu’ils sont utilisés avec, ou à la place, d’autres méthodes prophylactiques. Bien que la CPI soit désormais largement acceptée comme une forme valable de prophylaxie, ces anciennes études conservent toute leur valeur17. Voir les tableaux ci-dessous.
Études des résultats cliniques Flowtron
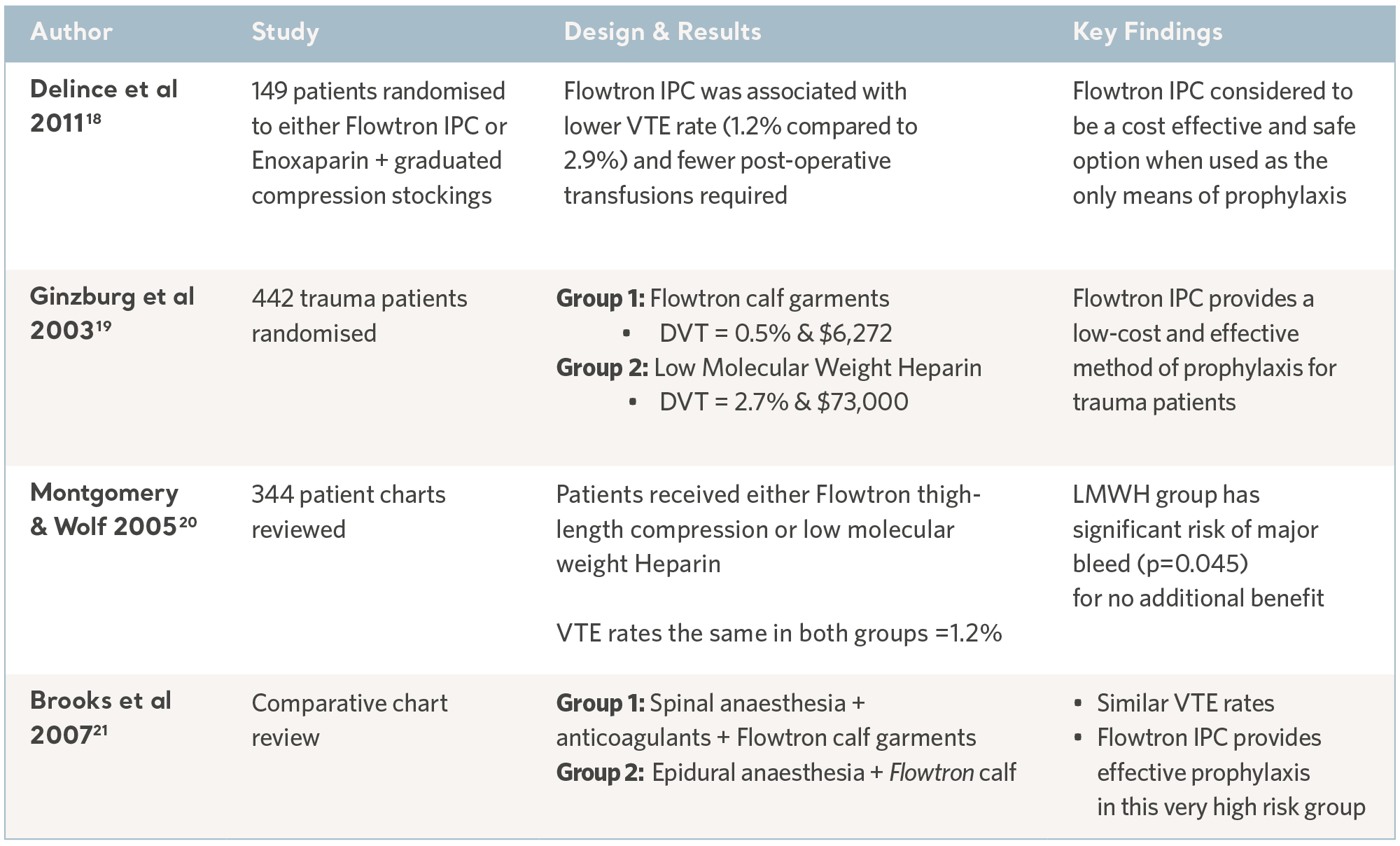
Données Flowtron dans les groupes spécialisés
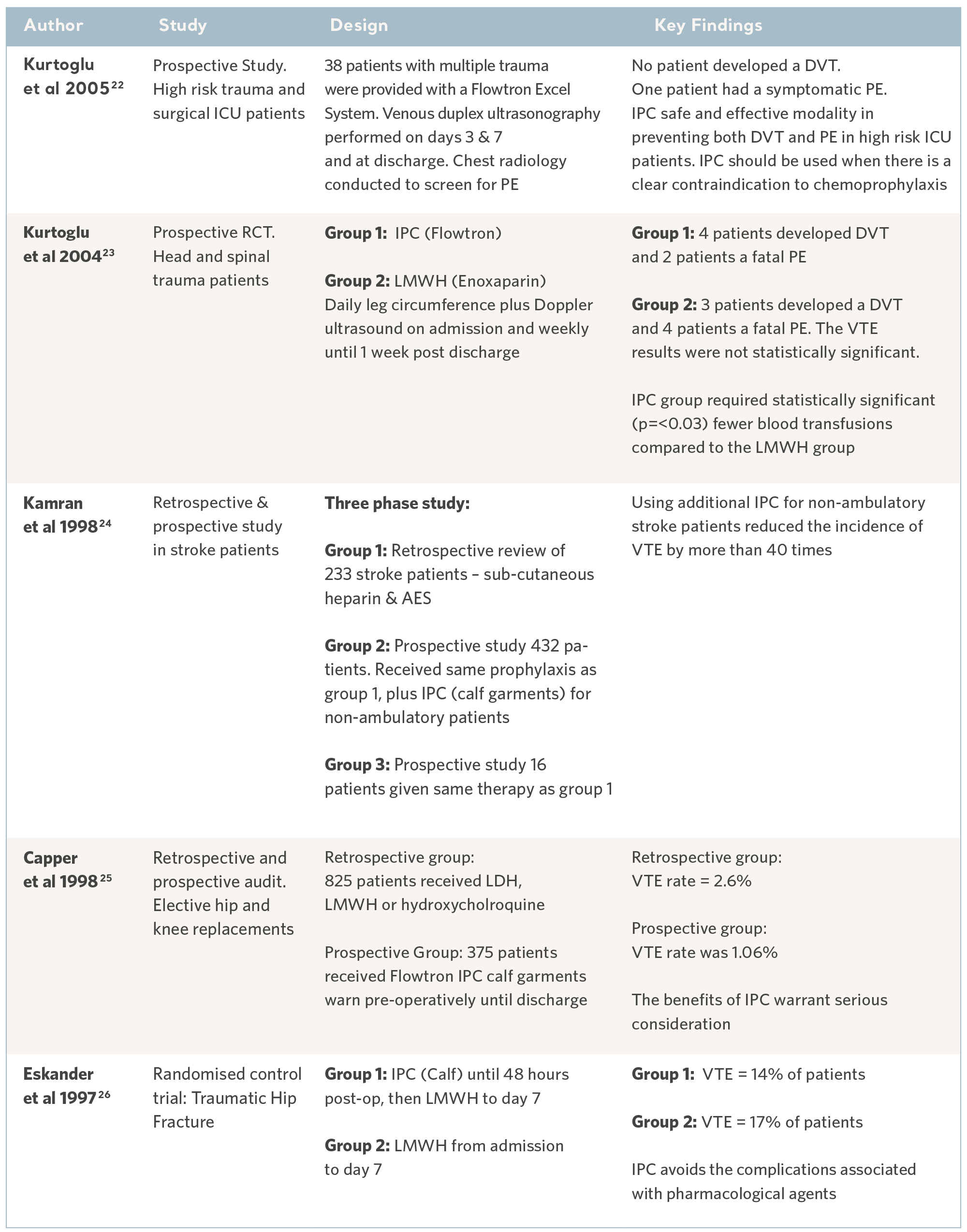
Données de CPI issues de la méta-analyse et d’examens systématiques
Comme dans toutes les interventions de prévention, la CPI s’avère uniquement efficace si elle est utilisée sur le bon patient au moment approprié. Il est donc primordial d’identifier les patients présentant un risque avant que la TEV n’apparaisse.
Parallèlement, le risque d’effets secondaires doit être pris en compte, notamment le risque d’hémorragie associé à l’utilisation d’un anticoagulant.
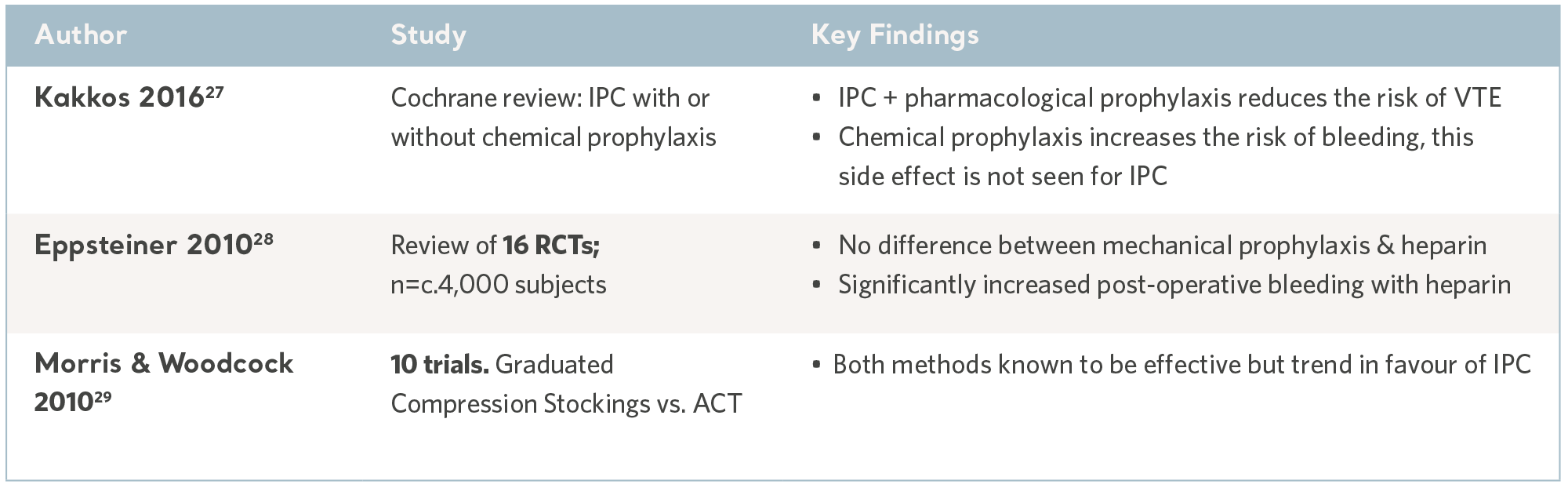
Les méta-analyses et examens systématiques, qui combinent différentes sources éprouvées en vue de déterminer l’utilité clinique globale de la CPI, constituent des sources d’informations utiles et orientent le médecin dans ses prescriptions.
Dans le prolongement de l’examen systématique, la publication des directives pratiques cliniques nationales et internationales traduit les recherches solides actuelles en recommandations distinctes : les lacunes sont comblées par des groupes de consensus internationaux. Même si leur formulation varie, les recommandations se veulent cohérentes et toutes désignent la CPI comme une intervention non seulement efficace, mais également sûre. Voir le tableau ci-dessous.
Données de CPI issues d’examens systématiques
Confort
À l’instar de toutes les méthodes de prophylaxie, la CPI se veut uniquement bénéfique si elle est correctement administrée et tolérée par les patients qui y recourent. En effet, le confort et la simplicité d’utilisation constituent des facteurs clés et la concordance peut varier.30
Au sein d’un environnement clinique très actif, le dispositif bénéficie d’une interface utilisateur intuitive et de fonctionnalités de sécurité appropriées visant à réduire le risque de blessures. Certains de ces aspects ont été évalués dans le cadre d’essais d’utilisation et d’évaluations technologiques indépendantes, notamment la sécurité, la qualité, la simplicité d’utilisation et le rapport coût-efficacité. Voir le tableau ci-dessous.
Données issues d’études d’utilisation 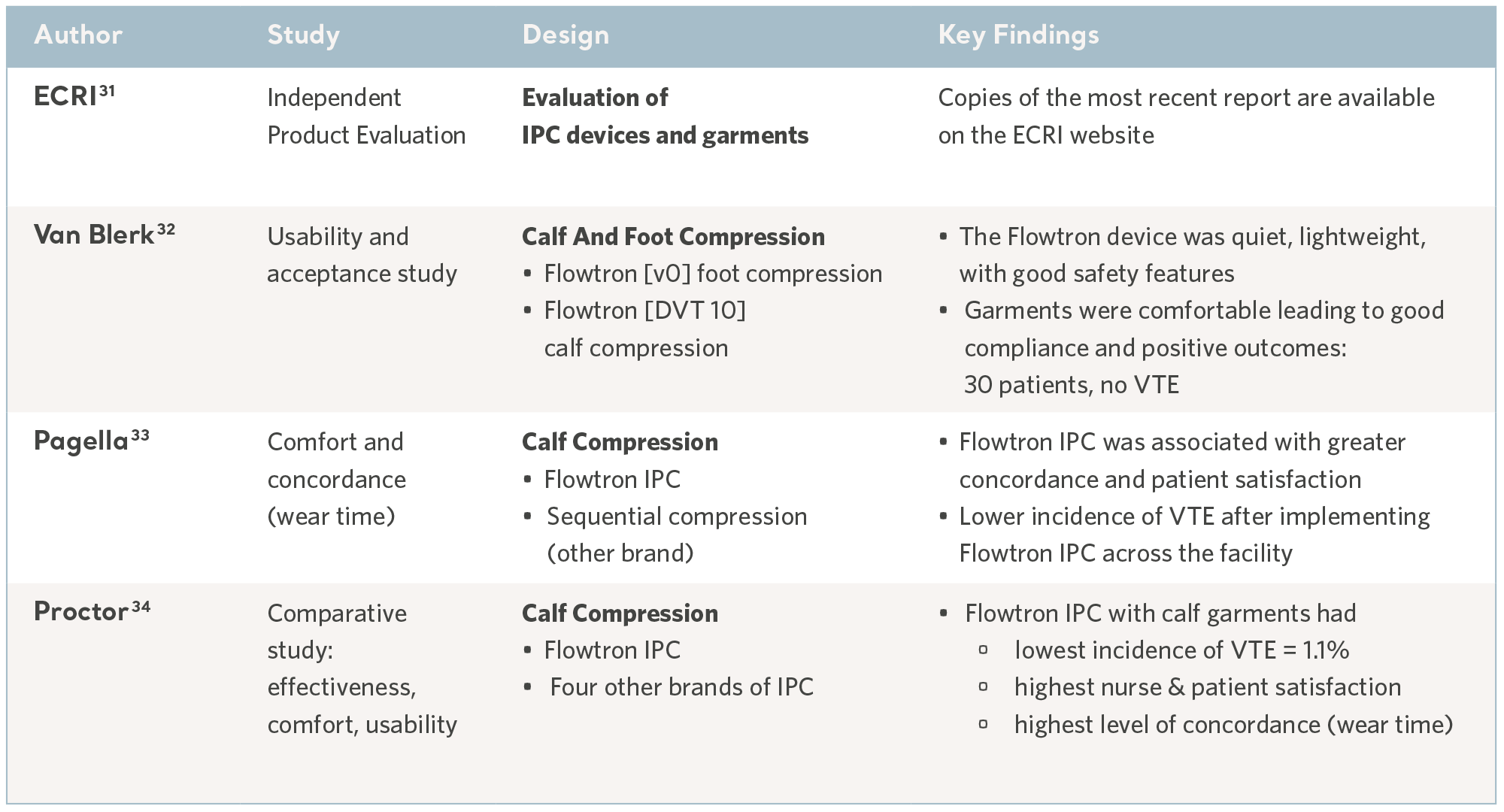
En savoir plus sur les données cliniques concernant la CPI Flowtron
Références
1- Beckman MG, Hooper WC, Critchley SE et al. Venous thromboembolism: a public health concern. Am J Prev Med. 2010; 38(4): S495-501.
2- Nelzen O, Bergqvist D, Lindhagen A. Leg ulcer etiology - a cross sectional population study. J Vasc Surg. 1991; 14: 557-64 cited in Nicolaides A, Fareed J, Kakkar A et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013; 32(2): 111-260.
3- Ruppert A, Steinle T, Lees M. Economic burden of venous thromboembolism: a systematic review. J Med Econ. 2011; 14(1): 65-74
4- Prevention and treatment of venous thromboembolism. Heart.org. https://www.heart.org/en/health-topics/venous-thromboembolism/prevention-andtreatmentof-venous-thromboembolism-vte. Dernière consultation en décembre 2019.
5- Jha AK, Larizgoitia I, Audera-Lopez C et al. The global burden of unsafe medical care: analytic modelling of observational studies. BMJ Qual Saf 2013; 22: 809-15.
6- Reitsma PH, Versteeg HH, Middeldorp S. Mechanistic view of risk factors for venous thromboembolism. Arteriosclerosis, thrombosis and vascular biology. 2012; 32(3): 563-8.
7- Nicolaides A, Fareed J, Kakkar A et al. Prevention and treatment of venous thromboembolism - International Consensus Statement. International Angiology. 2013;32(2): 111-260.
8- Guyatt GH, AKL EA, Crowther M et al. Executive Summary: Antithrombotic Therapy and Prevention of Thrombosis. 9th edition. American College of Chest Physicians. Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(2):7S-47S.
9- Pagella P, Cipolle M, Sacco E et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices. Orthop Nurs. 2007; 26(3):169-74.
10- Morris RJ, Giddings JC, Ralis HM, et aL. Haematological and haemodynamic comparison of the Kendall AV Impulse™ and the Arjo [Huntleigh] FP5000 Intermittent Pneumatic Foot Compression System. Arjo Clinical Report 2003.
11- Westrich G, Specht LM, Sharrock NE et al. Venous haemodynamics after total knee arthroplasty: evaluation of active dorsal to plantar flexion and several mechanical compression devices. The Journal of Bone & Joint Surgery. 1998; 80B(6): 1057-1066.
12- WoodcockJPandMorrisRJ.TheeffectoftheKendallSCDTMandArjo[Huntleigh]DVT30 garments on femoral and popliteal vein blood flow measurements. Arjo Clinical Report. 2002.
13- Flam E, Berry S, Coyle A et al. Blood flow augmentation of intermittent pneumatic compression systems used for the prevention of deep vein thrombosis prior to surgery. The American Journal of Surgery. 1996; 171(3): 312-315.
14- Flam E, Nackman G, Tarantino D et al. Intermittent pneumatic compression devices of the foot: a comparison of various systems on femoral vein blood flow velocity augmentation in the v supine and dependent, non-weight bearing positions. Arjo Clinical Report 2000.
15- Flam E, Berry S, Coyle A et al. DVT prophylaxis: comparison of two thigh high intermittent pneumatic compression systems. Présenté lors de l’assemblée de l’American College of Surgeons, San Francisco. 1993.
16- Morris RJ and Woodcock JP. Intermittent pneumatic compression for bariatric patients – the DVT60 compression garment. Arjo Clinical Report 2003.
17- Falck-Ytter Y, Francis CW, Johanson NA et al. Antithrombotic Therapy and Prevention of Thrombosis, 9th edition: ACCP Evidence Based Clinical Practice Guidelines: Prevention of VTE in Orthopedic Surgery Patients. Chest. 2012; 141: S2.
18- Delince P. RCT of intermittent pneumatic compression (IPC) versus low molecular weight heparin (LMWH) plus anti-embolic stockings (AES) in the prevention of venous thromboembolism during elective hip and knee surgery. Am. Ass. Orth. Surg. Conference 2011.
19- Ginzburg E, Cohn S, Lopez J et al. Randomised clinical trial of intermittent pneumatic compression and low molecular weight heparin in trauma. British Journal of Surgery. 2003; 90: 1338- 1344.
20- Montgomery JS and Wolf JS (2005). Venous Thrombosis Prophylaxis for Urological Laparoscopy: Fractionated Heparin versus Sequential Compression Devices. The Journal of Urology. 2005; 173: 1623-1626.
21- Brooks PJ, Keramati M, Wickline A . Thromboembolism in patients undergoing total knee arthroplasty with epidural analgesia. Journal of Arthroplasty. 2007; 22(5): 641-643.
22- Kurtoglu M, Guloglu R, Ertekin C et al. Intermittent pneumatic compression in the prevention of venous thromboembolism in high-risk trauma and surgical ICU patients. Turkish Journal of Trauma & Emergency Surgery. 2005; 11(1): 38-42.
23- Kurtoglu M, Yanar H et al. Venous thromboembolism prophylaxis after head and
spinal trauma: Intermittent pneumatic compression devices versus low molecular weight heparin. World Journal of Surgery. 2004; 28(8): 807-811.
24- Kamran SI, Downey D and Ruff RL. Pneumatic sequential compression reduces the risk of deep vein thrombosis in stroke patients. Neurology. 1998; 50(6): 1683- 1688.
25- Capper C. External pneumatic compression therapy for DVT prophylaxis. British Journal of Nursing. 1998; 7(14): 851-854.
26- Eskander M, Limb D, Stone M et al. Sequential mechanical and pharmacological thrombo prophylaxis in the surgery of hip fractures. International Orthopaedics. 1997; 21: 259-261.
27- KakkosSK, Caprini JA, Geroulakos G, et al.Combined intermittent pneumatic leg compression and pharmacological prophylaxis for prevention of venous thromboembolism. Cochrane Database of Systematic Reviews. Wiley & Sonds. 2016; 9. www.cochranelibrary.com
28- Eppsteiner RW, Shin JJ, Johnson J, van Dam RM. Mechanical compression versus heparin therapy in postoperative and post trauma patients: a systematic review and meta-analysis. World Journal of Surgery. 2010; 34(1): 10-19.
29- Morris RJ, Woodcock JP. Intermittent pneumatic compression or graduated compression stockings for deep vein thrombosis prophylaxis? A systematic review of direct clinical comparisons. Annals of Surgery. 2010; 251(3): 393-6.
30- Elpern E, Killeen K, Patel G, Senecal PA. Original Research: The Application of Intermittent Pneumatic Compression Devices for Thromboprophylaxis. AJN The American Journal of Nursing. 2013 Apr 1;113(4):30-6
31- ECRI Institute. March 2017 https://www.ecri.org/Pages/default.aspx
32- Van Blerk D. Evaluating an Intermittent Compression System for Thromboembolism Prophylaxis. Professional Nurse. 2004; 20(4): 48-49.
33- Pagella P, Cipolle M, Sacco E et al. A randomised trial to evaluate compliance in terms of patient comfort and satisfaction of two pneumatic compression devices.
Orthopaedic Nursing. 2007; 26(3): 169-174.
34- Proctor MC, Greenfield LJ, Wakefield TW et al. A clinical comparison of pneumatic compression devices: the basis for selection. Journal of Vascular Surgery. 2001; 34(3): 459-464.